近日,泌尿外科魏强教授团队与生物治疗全国重点实验室陈崇教授共同在Nature Reviews Urology(IF: 15.3)发表论文Targeting histone modifiers in bladder cancer therapy — preclinical and clinical evidence,系统阐述了靶向组蛋白修饰因子在膀胱肿瘤中的治疗潜力,总结了具有临床转化价值的相关靶点以及潜在生物学机制,同时探讨了目前相关临床试验的初步结果以及表观药物应用的挑战。

泌尿外科博士研究生张诗语为论文第一作者,泌尿外科魏强教授、谭平副教授,生物治疗全国重点实验室陈崇教授为共同通讯作者。我院为第一作者和通讯作者单位。
膀胱癌是泌尿系统常见的恶性肿瘤之一。目前占我国泌尿生殖系肿瘤发病率的第一位。尽管其他肿瘤的治疗方式在过去几十年中取得了飞速进展,但由于膀胱肿瘤异质性高等其他原因,膀胱癌的系统性治疗在进展相较缓慢。更好地理解膀胱癌的演化进化规律和分子机制,对明确用于早期预防膀胱癌复发或者应用于局部晚期和转移性膀胱癌的治疗靶点,或者寻找现有治疗增效策略以及指导临床试验的开展至关重要。
大量膀胱癌患者标本的全基因组和外显子序列测序结果表明,除了经典的肿瘤相关信号通路和基因扩增突变(PPARG, E2F3, EGFR, CCND1, MDM2等)及缺失突变(TP53,CDKN2A, RB1 等)以外,还有大量的表观遗传调控相关基因的异常表达。表观遗传调控重塑可能是膀胱癌发生和演进过程的重要驱动机制之一,并且可能作为潜在的治疗靶点。
传统的肿瘤治疗研究主要关注DNA序列改变(如基因突变、基因重排和拷贝数变异等)。与DNA序列中的发生永久性变化不同,通过修饰改变对染色质结构的灵活调整具有可逆的潜力。这种区别是表观遗传调控的基本特征,为潜在的“表观遗传疗法”奠定了基础。靶向功能增强的突变可以通过直接抑制进行干预,目前已经开发了许多小分子抑制剂,如组蛋白去乙酰化酶(HDAC)抑制剂、组蛋白甲基转移酶(HMT)抑制剂、BET抑制剂。靶向功能缺失的突变一直是我们面临的挑战,而在膀胱肿瘤中,结合大规模的测序结果推断,这些突变也恰恰可能是膀胱肿瘤发生的驱动因素。目前靶向缺失突变的主要手段包括:合成致死,靶向拮抗性调节因子等。临床前研究提示:单独靶向某一组蛋白修饰因子在膀胱肿瘤中有治疗效果,靶向组蛋白修饰因子联合其他治疗策略(例如AR 抑制剂,PARP抑制剂或者其他组蛋白修饰因子的抑制剂)值得关注。在本研究中,作者总结了处于临床前研究阶段用于靶向膀胱肿瘤中组蛋白修饰异常的小分子化合物、治疗靶点及研究模型。
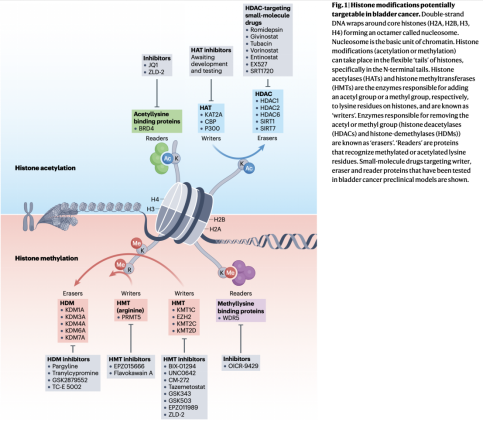
目前,仅少数小分子化合物进入临床试验且多数处于I/II期阶段。HDAC抑制剂是目前在膀胱癌临床试验中研究最多的表观药物,在局部晚期或者转移性膀胱癌患者中,表观单药治疗策略收效甚微且毒副反应较大。基于临床前研究,靶向组蛋白修饰因子对肿瘤免疫微环境具有调节作用,且表观药物联合免疫治疗在许多临床前膀胱癌模型中取得了显著的治疗效果,数个临床试验因此发起,初步结果提示多数病人对治疗响应且耐受。因此,与经典疗法(化疗、免疫治疗等)联合应用或成为更好的治疗策略。

作者讨论了靶向表观遗传修饰因子在实体肿瘤治疗中的挑战,同时对未来亟待解决的问题做出展望,呼吁更多处于临床前基础或转化研究中的相关靶点和小分子化合物进入临床试验,为膀胱癌患者带来更多可能的获益。