bemarituzumab(bema)联合mFOLFOX6对比安慰剂联合mFOLFOX6一线治疗晚期胃/胃食管交界癌的随机双盲研究(FIGHT)
研究背景:
成纤维细胞生长因子受体2b(FGFR2b)是FGFR家族(FGFR1-4)的一员,是FGFR2的剪接异构体,约3-61%的胃癌患者存在FGFR2b过表达,FGFR2b过表达比例取决于肿瘤分期和检测。FGFR酪氨酸激酶抑制剂在FGFR突变、融合或易位的肿瘤中显示出临床疗效。Bemarituzumab是一种针对FGFR2b受体的特异性IgG1抗体,Bemarituzumab选择性地与FGFR2b结合,抑制配体结合,介导抗体依赖性细胞介导的细胞毒作用。前期的研究(纳入28例患者)发现Bemarituzumab单药治疗后线治疗的FGFR2b阳性的晚期胃癌,其ORR为18%,未见剂量限制性毒性,角膜不良事件发生率为3/28,第2阶段推荐剂量:第1周期第8天给药7.5mg/kg,后续周期15 mg/kg,每2周为一周期。
研究设计:
该研究主要纳入的既往未经治疗的不可切除的局部晚期或转移性胃腺癌/胃食管交界处腺癌,并且有RECIST v1.1可评估的病灶;且IHC检测FGFR2b过表达和/或ctDNA检测FGFR2基因扩增,并且ECOG PS评分为0或1分,且患者HER2检测阴性,并且至少可以接受1次剂量的mFOLFOX6方案的化疗。研究最初计划是一项纳入550例的III期临床研究[1],最终在入组了155例患者后,修正为了II期临床研究。研究按照1:1的比例随机分为试验组(接受Bemarituzumab+ mFOLFOX6,每两周为一周期)和对照组(接受安慰剂+ mFOLFOX6,每两周为一周期)。研究的分层因素包括:地理区域,筛选期间接受1次剂量mFOLFOX6化疗,既往接受过辅助或新辅助治疗。研究主要终点为研究者评估的PFS,次要终点为OS和ORR,具体研究设计见图1。
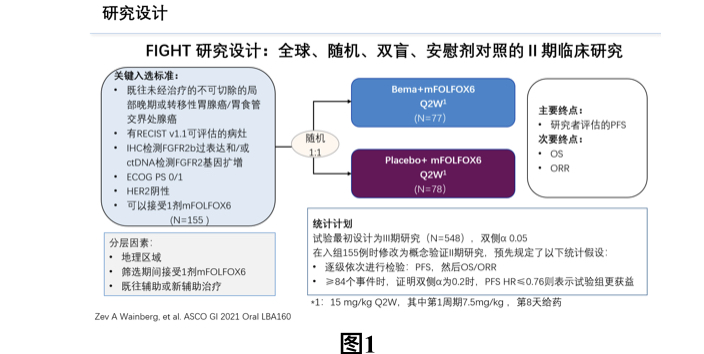
研究结果:
FIGHT研究入组期限从2018年9月28日至2020年5月12日,此次公布的数据截止日期为2020年9月23日,中位随访时间为10.9个月(范围,0.03-0.22)。研究共计筛选910例患者,最终纳入155例患者(FGFR2b+患者约占30.2%),试验组77例,对照组78例。两组患者的基线状态按分层因素匹配平衡。尽管FGFR2b通过IHC、ctDNA任一种方式确认阳性均可入组,但绝大多数患者(83.2%)是IHC+,ctDNA阴性的患者,见图2。
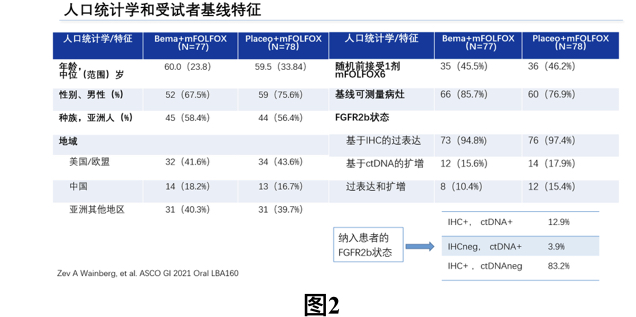
研究的主要观察终点PFS方面,试验组和对照组的中位PFS分别为9.5个月和7.4个月(P=0.0727),次要终点OS:试验组中位OS尚未达到,对照组中位OS为12.9个月(P=0.0268),HR为0.58(0.35,0.95),试验组患者的OS具有统计学意义上的延长,具体见图3。ORR方面,为47%(试验组)对比33%(对照组),且试验组2例患者达到CR,对照组无CR患者;分析基线具有可测量病灶的126例患者而言,两组ORR分别为53%(试验组)对比40%(对照组);对于达到客观疗效的患者而言,两组患者中位TTR无明显差异,但试验组患者显示出更长的中位疗效持续时间,为12.2个月(试验组)对比7.1个月(对照组),见图4。
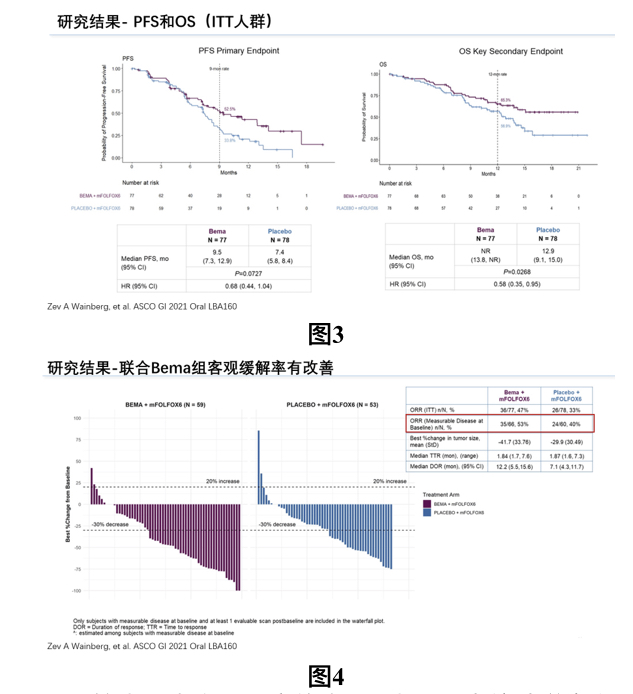
尽管本研究主要观察终点PFS未显示出统计学意义上的差异,但亚组分析发现,PFS与FGFR2b表达高低成正相关,对于FGFR2b的IHC检测为2+/3+的患者而言,两组患者的9个月PFS率上分析,试验组显示了更高的9个月PFS率,见图5。此外,OS也与FGFR2b表达高低成正相关,不仅对于ITT人群,试验组显示了更长的OS,对于FGFR2b的IHC检测为2+/3+的患者来说,试验组患者的1年OS率均明显高于对照组患者,见图6。
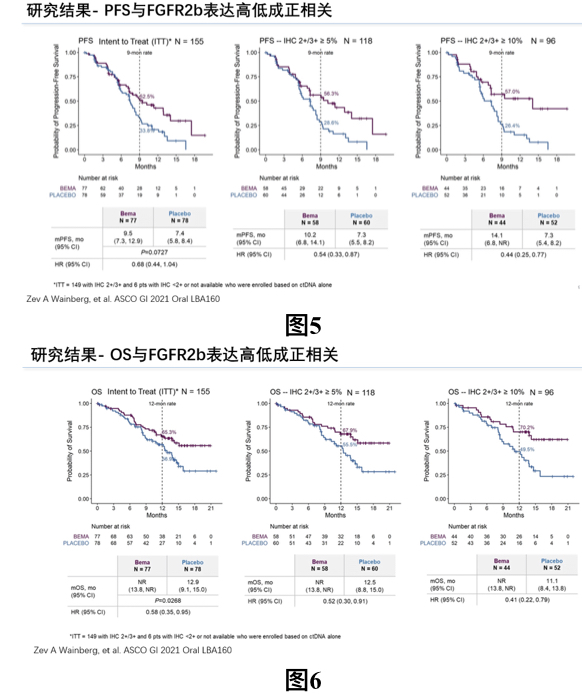
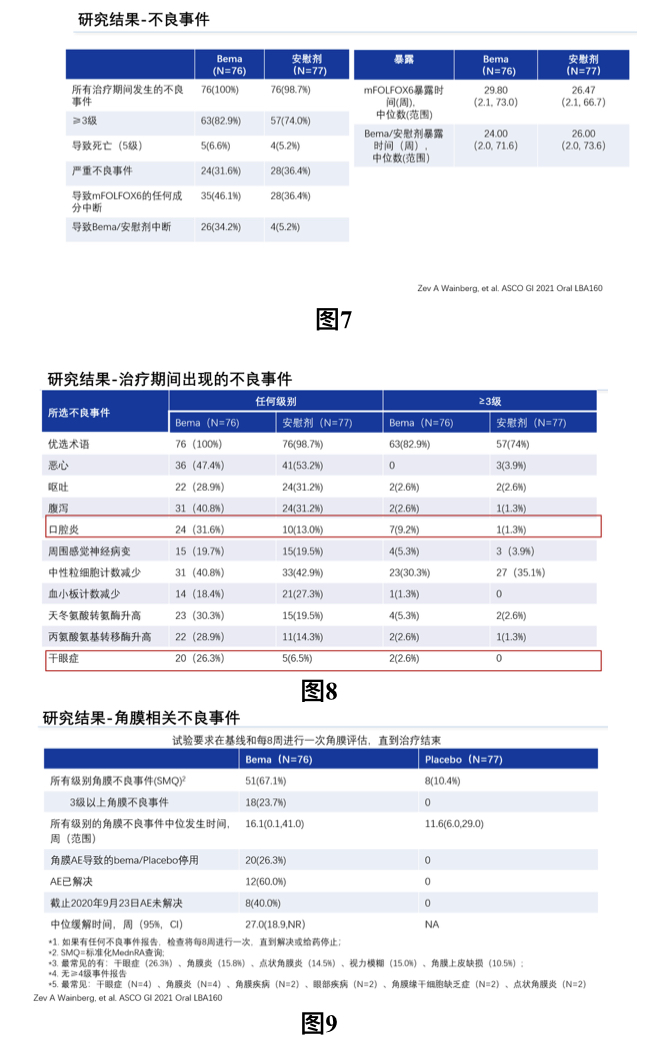
不良事件方面,两组患者所有治疗期间的不良事件发生率相似,100%对比97%。试验组患者≥3级的不良事件发生率更高,82.9%对比74%;导致死亡的不良事件分别为5例(试验组)和4例(对照组)。两组患者的严重不良事件发生率分别为31.6%(试验组)和36.4%(对照组);试验组患者Bemarituzumab/安慰剂中断的比例更高,分别为34.2%(试验组)和5.2%(对照组);两组患者的中位药物暴露时间无显著差异,见图7。除常见的化疗不良反应外,试验组患者较对照组患者的口腔炎和干眼症的发生比例均更高,≥3级的口腔炎发生比例也更高,见图8。此外,该研究要求在基线和每8周对患者进行一次角膜评估,直到治疗结束,并最终发现试验组患者的所有级别角膜不良事件发生率以及3级以上角膜不良事件发生率均显著高于对照组,见图9。
研究结论:
FIGHT试验是第一个针对靶向FGFR2b过表达的胃/胃食管腺癌的前瞻性随机II期研究;该研究通过中心实验室进行IHC检测,发现一线晚期非HER2阳性胃癌/胃食管交界处腺癌中FGFR2b阳性的患者约占30%;Bemarituzumab与mFOLFOX6化疗联合应用,可改善PFS, OS和ORR;Bemarituzumab与角膜不良事件和口腔炎的增加有关,大多数是可逆的。
专家点评:
对于不可手术切除的晚期胃癌而言,奥沙利铂联合氟尿嘧啶类药物的化疗方案仍是目前可选的标准方案之一。然而,化疗的有效率和对患者的生存改善仍相对有限。成纤维细胞生长因子受体(FGFRs)是跨膜酪氨酸激酶受体,并通过与其配体结合从而激活下游PI3K-AKT和MAPK-ERK通路[2]。FGFR2通路的激活也是胃癌发生发展的重要途经[3],据报道,FGFR2b 过表达/FGFR2扩增的比例可达10%,也为靶向FGFR2b 的抗体治疗提供了理论依据[1]。在FGFR2扩增的胃癌中,主要是FGFR2b亚型的过表达[4]。FGFR酪氨酸激酶抑制剂在FGFR突变、融合或易位的肿瘤中已显示出临床疗效,其中Bemarituzumab是一种针对FGFR2b受体的特异性IgG1抗体,在一项评估Bemarituzumab在FGFR2b过表达胃和胃食管交界腺癌(GEA)患者中的安全性、药代动力学和初步疗效的I期剂量爬升试验中,Bemarituzumab耐受性良好,在晚期胃和胃食管交界腺癌患者中,单药治疗显示出了疗效并也确认了后续研究的安全剂量[4]。FIGHT研究正是基于I期研究基础上设计的全球、随机、双盲、安慰剂对照的Ⅱ期临床研究,也是第一项纳入局部晚期或转移性胃腺癌/胃食管交界处腺癌患者探索靶向FGFR2b疗效的随机对照研究。因此,进一步探索Bemarituzumab在FGFR2b过表达和/或FGFR2基因扩增的晚期胃和胃食管交界腺癌患者中的疗效十分重要,FIGHT研究从研究设计上与TOGA研究设计相似[5],也是纳入特定基因表达的患者,在标准化疗的基础上探索加或不加靶向药物是否能使患者获益的随机对照研究。FIGHT研究也是纳入FGFR2阳性的这部分患者,并且在一线治疗时与标准的奥沙利铂联合氟尿嘧啶类药物的化疗方案相组合,既符合伦理的需求,又进一步为验证Bemarituzumab在一线治疗时的价值提供了宝贵数据。
尽管FIGHT研究的主要观察终点PFS并未显示出统计学意义上的差异,但试验组仍显示出了PFS延长的趋势,试验组和对照组的中位PFS分别为9.5个月和7.4个月(P=0.0727),亚组分析也发现PFS与FGFR2b表达高低成正相关,FGFR2b为2+/3+的亚组患者,试验组显示了更高的9个月PFS率,无论是ITT人群还是亚组人群的分析,两组患者的生存曲线随着随访时间的延长也显示出了进一步分离的趋势,或许随着随访时间的延长,两组患者的PFS也能够显示出统计学意义上的差异。次要终点OS和ORR方面,试验组也显示出了明显的优势,Bemarituzumab能够在标准化疗基础上进一步提供疗效,改善患者生存。除了常见的化疗相关不良反应外,口腔炎和角膜不良事件在试验组的发生显著升高,这也是Bemarituzumab相对特殊的毒性反应,但总体而言,大多数患者的毒性均为可逆性和可控制。但是同样也需要注意,在两组患者中,分别有5例和4例药物导致死亡的不良事件发生,这些安全性数据也为后续开展更大样本的III期临床提供了信息。
目前,随着NGS越来越广泛地应用于晚期肿瘤患者,为患者提供个体化治疗。尽管FGFR2如同HER2一样,在胃腺癌/胃食管交界处腺癌患者中的表达并不十分常见,但是能够通过个体化的检测手段,找到这样的分子信息,为患者提供精准的靶向治疗的确是现在基因指导下的个体化治疗中的进行临床研究的发展趋势。从这项II期研究中,我们已经初步观察到了Bemarituzumab的疗效和毒性谱,也期待其III期研究能够结合标志物筛选或者剂量调整等信息进一步确认Bemarituzumab的疗效和安全性,能够像“曲妥珠单抗”一样为特定基因表达的人群提供可靠的靶向治疗。
专家介绍:


参考文献:
1. Catenacci DV, Tesfaye A, Tejani M, Cheung E, Eisenberg P, Scott AJ, Eng C, Hnatyszyn J, Marina N, Powers J, Wainberg Z (2019) Bemarituzumab with modified FOLFOX6 for advanced FGFR2-positive gastroesophageal cancer: FIGHT Phase III study design. Future oncology (London, England) 15 (18):2073-2082. doi:10.2217/fon-2019-0141
2. Katoh M, Katoh M (2006) FGF signaling network in the gastrointestinal tract (review). International journal of oncology 29 (1):163-168
3. Xie L, Su X, Zhang L, Yin X, Tang L, Zhang X, Xu Y, Gao Z, Liu K, Zhou M, Gao B, Shen D, Zhang L, Ji J, Gavine PR, Zhang J, Kilgour E, Zhang X, Ji Q (2013) FGFR2 gene amplification in gastric cancer predicts sensitivity to the selective FGFR inhibitor AZD4547. Clinical cancer research : an official journal of the American Association for Cancer Research 19 (9):2572-2583. doi:10.1158/1078-0432.Ccr-12-3898
4. Catenacci DVT, Rasco D, Lee J, Rha SY, Lee KW, Bang YJ, Bendell J, Enzinger P, Marina N, Xiang H, Deng W, Powers J, Wainberg ZA (2020) Phase I Escalation and Expansion Study of Bemarituzumab (FPA144) in Patients With Advanced Solid Tumors and FGFR2b-Selected Gastroesophageal Adenocarcinoma. Journal of clinical oncology : official journal of the American Society of Clinical Oncology 38 (21):2418-2426. doi:10.1200/jco.19.01834
5. Bang YJ, Van Cutsem E, Feyereislova A, Chung HC, Shen L, Sawaki A, Lordick F, Ohtsu A, Omuro Y, Satoh T, Aprile G, Kulikov E, Hill J, Lehle M, Rüschoff J, Kang YK (2010) Trastuzumab in combination with chemotherapy versus chemotherapy alone for treatment of HER2-positive advanced gastric or gastro-oesophageal junction cancer (ToGA): a phase 3, open-label, randomised controlled trial. Lancet 376 (9742):687-697. doi:10.1016/s0140-6736(10)61121-x