
2月27日,四川大学华西医院生物治疗研究中心汪源/张燕研究员团队,联合清华大学/北京卓凯生物马伟伟博士、江西科技师范大学王松华副教授团队,在肿瘤学国际顶级期刊Cancer Discovery(IF:33.3)在线发表题为“Glioblastoma-secreted C1QL1 orchestrates tumor microtube expansion and neural synaptic pruning to drive malignant synapse formation and recurrence”的研究论文,发现胶质母细胞瘤(GBM)分泌的C1QL1是介导肿瘤—肿瘤、肿瘤—神经元通讯的关键信号分子,靶向C1QL1-BAI3-Rac1可同时阻遏TM和恶性突触形成、抑制肿瘤复发。
四川大学华西医院为本论文第一作者单位和第一通讯作者单位;清华大学/北京卓凯生物钟毅教授、首都医科大学北京天坛医院张伟教授为本研究提供了大力支持和帮助。
胶质母细胞瘤(GBM)是最常见、恶性程度最高的原发性脑肿瘤,患者预后极差。GBM呈现广泛的浸润性生长,浸润区肿瘤细胞难以通过手术+放化疗清除,是耐药和复发的重要原因。近年的研究表明,GBM细胞在侵袭初始阶段互不相连,但在定植后可生长出神经突样的肿瘤微管(TM)相互连接形成肿瘤网络,并与正常神经元形成功能突触(恶性突触),利用神经活动产生的电信号和旁分泌信号促进肿瘤生长、耐药和复发。然而,浸润区胶质瘤细胞如何通过肿瘤细胞间通讯促进TM和肿瘤网络形成、如何与正常突触竞争形成恶性突触的分子机制尚不清楚,核心信号分子尚不明确,也缺乏有效的干预策略。
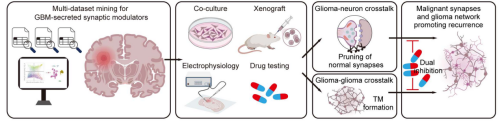
研究团队整合多组GBM单细胞与空间转录组数据,发现C1QL1在肿瘤浸润区高电活动的GBM OPC-like细胞中特异性高表达,与患者不良预后、短复发时间相关,在多种GBM模型中证实其为关键促癌因子。进一步研究表明,C1QL1 调控肿瘤及肿瘤—神经元互作,促进肿瘤细胞间TM形成、正常神经元突触修剪及神经元—胶质瘤恶性突触形成。机制上,C1QL1与GBM细胞及神经元的BAI3受体结合,激活Rac1信号促进细胞骨架重排,在GBM中诱导TM形成,在神经元中诱导突触修剪,进而推动恶性突触形成。
清华大学/北京卓凯生物钟毅/马伟伟团队前期开发了一款国产First-in-class 非GEF靶向的Rac1抑制剂JK50561,相较于已报道的Rac1抑制剂具有高效低毒、高血脑屏障通透性等优势,也是目前全球唯一完成阿兹海默症治疗临床二期试验的Rac1抑制剂,临床数据显示良好的安全性和有效性。研究团队测试发现JK50561能有效抑制GBM中TM的形成,挽救GBM诱导的神经突触修剪,抑制恶性突触形成。在GBM术后复发模型中也可抑制肿瘤复发、延长生存期,还能阻遏相关通路及肿瘤相关神经元异常活动,与放疗联用可协同抑制复发。
综上,本研究发现C1QL1作为浸润区GBM细胞分泌的核心信号因子,通过强化肿瘤网络(TM形成)、重塑神经环路(神经突触修剪)的双重作用驱动GBM复发,揭示了浸润区GBM的调控新机制和靶向策略。
该研究获得国家自然科学基金、国家科技部重点研发、四川省科技厅及华西医院“1·3·5”计划等多项基金支持。
原文链接:https://doi.org/10.1158/2159-8290.CD-25-1123