2月24日,我院生物治疗科刘继彦教授团队联合华西第二医院病理科沈扬眉教授、西南财经大学统计与数据科学学院刘斌教授团队在人工智能与医学交叉领域国际权威期刊npj Digital Medicine杂志发表文章“Distinction between primary and metastatic mucinous ovarian carcinoma from histopathology images using deep learning”。团队基于H&E全切片病理图像开发了深度学习模型MOCOPM,首次实现AI对原发性与消化道转移性卵巢粘液癌的自动精准鉴别,为临床妇科病理诊断提供了新的辅助工具。
四川大学华西医院为本论文第一作者单位和第一通讯作者单位;我院生物治疗科刘继彦教授以及华西第二医院病理科沈扬眉教授为共同通讯作者;我院生物治疗研究中心张明逸博士后以及西南财经大学统计与数据科学学院刘斌教授为文章的共同第一作者。
卵巢黏液癌(MOC)是卵巢上皮性癌的重要组织学亚型之一,可分为原发性MOC和来源于胃肠道的转移性黏液癌,两者在治疗策略和预后方面存在显著差异。然而,目前的病理鉴别方法仍存在一定局限,如对病理医师经验依赖较高、诊断过程耗时且经济成本较高等。此外,在临床实践中,患者常缺乏明确的胃肠道肿瘤病史使得鉴别更加困难。因此,探索更加高效、精准的辅助诊断方法具有重要意义。
本研究提出假设:深度学习模型能够从常规H&E染色病理切片中自动提取区分原发性与胃肠道转移性MOC的关键形态特征,从而辅助判断肿瘤来源。围绕这一问题,研究团队构建了基于深度学习的MOC来源预测模型(MOCOPM),并系统评估其在鉴别原发性与转移性卵巢黏液癌中的诊断性能。
研究共纳入167例原发性或胃肠道转移性MOC患者,共337张H&E染色全切片图像。其中131例用于模型训练及内部五折交叉验证,36例用于独立外部验证,并引入UBC-OCEAN公开数据库中的40例相关病理图像进行额外验证。研究比较了三种深度学习模型架构,包括ResNet-18、EfficientNet-B1以及结构感知分层图多实例学习框架(SGMF),最终选择表现最佳的SGMF构建MOCOPM模型。同时利用GNNExplainer进行可解释性分析,以识别模型关注的关键病理区域。
研究结果显示,基于SGMF架构构建的MOCOPM模型在区分原发性与胃肠道转移性MOC方面表现良好:在内部验证数据集中AUROC为0.91,在外部独立验证数据集中AUROC为0.96,显示出较好的泛化能力。可解释性分析表明,模型关注的区域与妇科病理学家常用的诊断特征高度一致,如印戒细胞聚集、侵袭性生长模式以及良恶性成分共存等。此外,团队还建立了在线辅助诊断平台(http://www.aislide.clinic),用户可上传H&E染色病理切片图像并获得MOCOPM模型的示例分类结果,进一步展示了该模型的应用潜力。
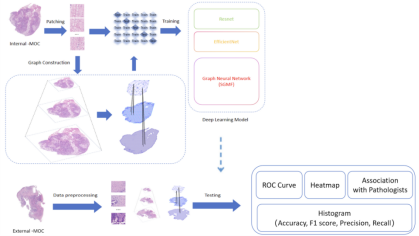
MOCOPM深度学习模型构建流程图