我院腹部肿瘤病房马骥副教授团队近期在Cancer Communications(IF:16.2)发表研究文章The crosstalk between ferroptosis and anti-tumor immunity in the tumor microenvironment: molecular mechanisms and therapeutic controversy,系统阐述了肿瘤微环境中铁死亡与抗肿瘤免疫的通路串扰机制:从肿瘤细胞和肿瘤浸润免疫细胞两个角度,总结了目前关于铁死亡与抗肿瘤免疫的相互矛盾的观点及通路调控的相互影响,探讨铁死亡在肿瘤免疫治疗中的前景与挑战。
我院硕士研究生郑义琛为第一作者,腹部肿瘤病房马骥副教授为通讯作者,我院为第一作者和通讯作者单位。

铁死亡在癌症治疗领域一直受到广泛关注,通常认为诱导铁死亡具有治疗耐药肿瘤和增强免疫治疗疗效的潜力。近年来部分研究发现铁死亡可能会抑制抗肿瘤免疫而促进肿瘤进展。因此有必要对相关研究进行综述以探讨铁死亡在肿瘤免疫治疗中的前景与挑战。
一.从癌细胞的角度看铁死亡与抗肿瘤免疫的串扰
免疫原性细胞死亡(ICD)是一种特定类型的细胞死亡,能够激活免疫系统并与免疫治疗协同作用。之前的不少研究均提示铁死亡属于ICD,因为有大量证据表明铁死亡的癌细胞能够释放损伤相关分子模式(damage-associated molecular patterns,DAMPs),其为ICD最显著的特征,能够作为佐剂增强免疫反应。然而,ICD的另外两大特征——细胞因子的释放及抗原性的调节上,铁死亡却缺乏足够的证据。在检验ICD的金标准——预防性疫苗接种模型上,目前存在相矛盾的结论,最近的研究认为铁死亡不属于ICD且会抑制抗肿瘤免疫。
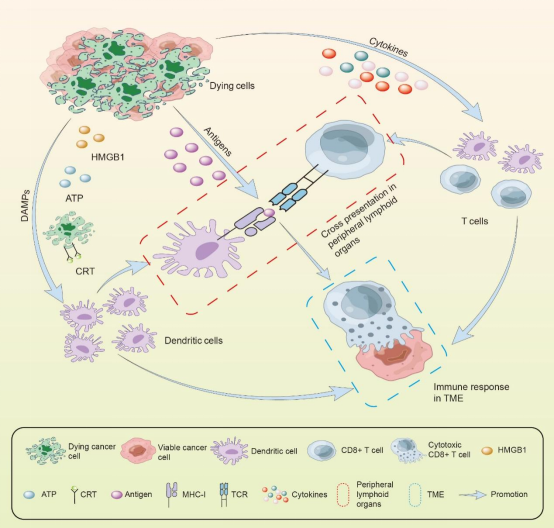
图1 ICD的三大特征
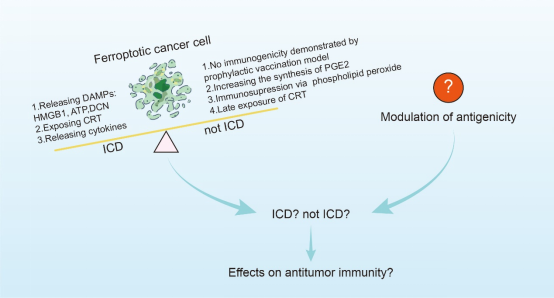
图2 铁死亡是否属于ICD仍有争议
研究关于铁死亡癌细胞对抗肿瘤免疫的具体作用也存在矛盾。其能通过表达SAPE-OOH这种特殊的磷脂促进巨噬细胞对其的吞噬,能激活NK细胞并促进干扰素γ(interferon-γ,IFN-γ)的释放等不同的机制促进抗肿瘤免疫。其也能通过释放8-羟基鸟苷、KrasG12D蛋白促进巨噬细胞向促肿瘤的M2型极化,能通过上调环氧合酶2(cyclooxygenase 2,COX-2)的表达增加免疫抑制的前列腺素E2的合成等机制抑制抗肿瘤免疫,具体发挥何种作用,可能取决于特定的肿瘤类型和具体的环境。

图3 铁死亡癌细胞对抗肿瘤免疫的作用
二.从免疫细胞的角度看铁死亡与抗肿瘤免疫的串扰
免疫治疗激活的CD8+T细胞能通过分泌IFN-γ促进肿瘤细胞铁死亡,发挥杀伤肿瘤细胞的作用。这是一种新发现的CD8+T细胞杀伤肿瘤的机制(之前主要认为是穿孔素-颗粒酶和 Fas-FasL途径),也为联合免疫治疗与铁死亡靶向治疗奠定了理论基础。
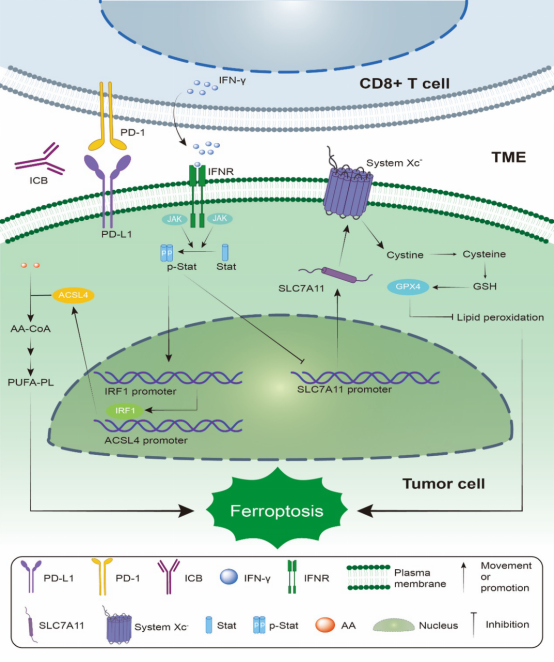
图4 CD8+ T 细胞通过铁死亡杀死癌细胞
然而,在使用铁死亡诱导剂杀伤肿瘤细胞的同时,其对免疫细胞的影响也不可忽视。例如,CD8+T细胞对GPX4(铁死亡诱导剂)的敏感性比癌细胞更强,在GPX4尚未杀伤肿瘤时便已经损害了抗肿瘤免疫。但其对Xc-系统抑制剂(另一种铁死亡诱导剂)却并不敏感。类似的,铁死亡诱导也可能损害其他抗肿瘤免疫细胞(如树突状细胞和NK细胞)的功能,而发挥促肿瘤作用的髓系来源抑制细胞(MDSCs)却对铁死亡相对不敏感,因而可能发挥免疫抑制的作用。不过铁死亡诱导也可以损害免疫抑制细胞的功能,起到一定程度的抗肿瘤作用。例如,Treg细胞对GPX4高度敏感、铁死亡诱导可以促进肿瘤相关巨噬细胞(TAMs)向抗肿瘤的M1表型转化等。
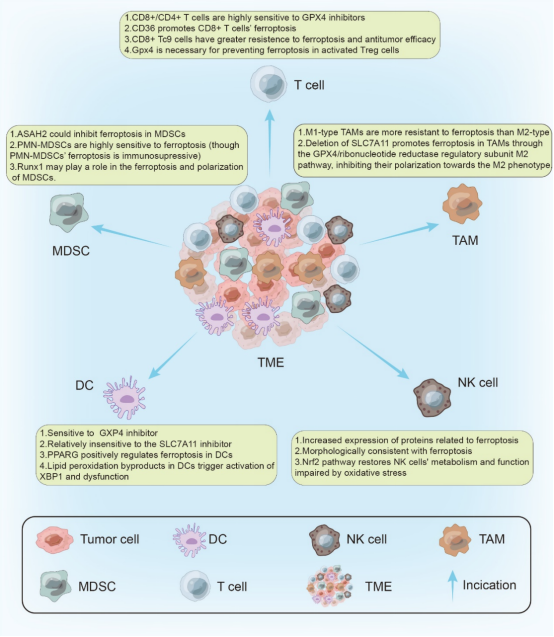
图5 TME中的免疫细胞对铁死亡的敏感性
另外,铁死亡的免疫细胞不仅会丧失其原本的功能,甚至可能获得免疫抑制的功能。例如多形核MDSC(PMN-MDSC)对铁死亡高度敏感并自发发生铁死亡,但这反而上调了其PGE2的合成而增强了其免疫抑制作用,促进肿瘤进展。
三.展望
1.虽然现有证据存在矛盾,但铁死亡促进抗肿瘤免疫的直接证据相对更充分,而支持铁死亡抑制抗肿瘤免疫的证据则更多聚集在局部机制上的研究。铁死亡癌细胞对抗肿瘤免疫的整体作用可能取决于瘤种的不同及具体的环境,但在总体上其对抗肿瘤的促进作用可能要比抑制作用更强一些。不过,仍需进一步的研究以获得更多相关证据并阐明背后机制仍是必要的,这样有助于明确铁死亡促进或抑制抗肿瘤免疫的具体条件,并在将来提供针对性的方法扩大其正向作用并减弱其负面效果。
2. 抗肿瘤免疫细胞的铁死亡及相关的功能减弱可能在部分铁死亡介导的免疫抑制中发挥着重要作用。但介导不同免疫细胞间铁死亡敏感性的关键分子及信号通路可能存在差异,这为铁死亡的靶向治疗提供了可能,甚至能因而利用铁死亡杀伤免疫抑制细胞群。此外,将抗肿瘤免疫细胞进行抗铁死亡修饰后再联合铁死亡治疗可能是一种可行方法。
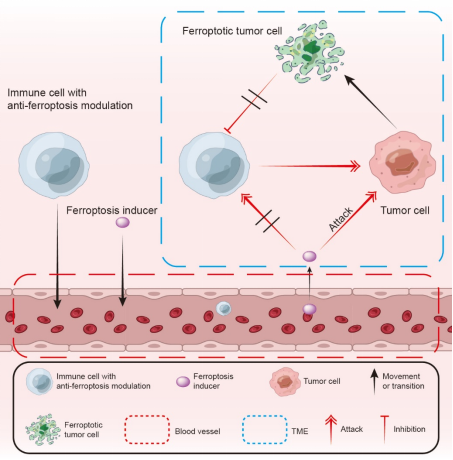
图6 铁死亡靶向疗法与过继细胞疗法的可能组合
3.鉴于铁死亡与脂质代谢的密切关系,及脂质代谢产物在免疫调控中的重要作用,脂质代谢可能在铁死亡与抗肿瘤免疫的相互作用中发挥着密切作用。
4.目前关于铁死亡是否属于ICD的关键证据仍不充分,其可能直接影响不同免疫表型TME铁死亡靶向治疗联合免疫治疗的直接策略,仍需进一步研究。
经过系统梳理,研究认为铁死亡与抗肿瘤免疫之间的关系是复杂的。虽然铁死亡癌细胞对抗肿瘤免疫的总体影响可能因肿瘤类型和特定环境而异,但总体来看其对抗肿瘤活性的促进作用要更强一些;仍需更多研究阐明铁死亡癌细胞的免疫原性、铁死亡对免疫细胞的影响以及铁死亡细胞与抗肿瘤免疫的相互作用,以进一步阐明铁死亡在抗肿瘤免疫中的调节作用及其潜在机制。这将有助于明确铁死亡靶向治疗肿瘤的可行性和潜在缺陷,为针对不同类型肿瘤选择铁死亡靶向治疗和免疫治疗的不同联合策略提供转化依据。